Medicina rigenerativa dell'ischemia miocardica e periferica
Unità di Biologia vascolare e Medicina rigenerativa. Responsabile Giulio Pompilio
⇒ Ruolo dei progenitori cardiaci umani (hCPCs) nell’omeostasi miocardica e loro utilizzo come prodotti di terapia biologica avanzata. Profilo clinico e farmaci
⇒ Studio dei meccanismi epigenetici e molecolari della disfunzione dei progenitori vascolari nelle patologie metaboliche
⇒ Studi pre-clinici di prodotti di terapia cellulare cardiaca e traslazione clinica GMP-grade
Ruolo dei progenitori cardiaci umani (hCPCs) nell’omeostasi miocardica e loro utilizzo come prodotti di terapia biologica avanzata. Profilo clinico e farmaci
La scoperta di progenitori residenti nel cuore adulto ha rivoluzionato il dogma del cuore come organo incapace di autorinnovamento. Il nostro e altri gruppi di ricerca abbiamo dimostrato la presenza di una popolazione di cellule progenitrici residenti cardiache (hCPCs) in grado di differenziare in cardiomiociti, cellule endoteliali e cellule muscolari lisce in-vitro e in-vivo, contribuendo all’omeostasi tissutale e alla rigenerazione cardiaca.
Per studiare il ruolo delle hCPCs nell’omeostasi fisiopatologica nel cuore umano, l’Unità ha interesse nella correlazione tra il profilo clinico e terapeutico dei pazienti cardiopatici e le caratteristiche biologiche delle hCPCs (Gambini et al. Transl Res 2012). I nostri risultati hanno mostrato che alcune variabili cliniche del paziente (per es. fattori di rischio cardiovascolari e la terapia farmacologica) hanno un impatto sul numero e la funzione delle hCPCs residenti.
Gli studi in corso sono volti a valutare l'influenza di alcuni farmaci sulla proliferazione, sul differenziamento, sulla risposta allo stress ossidativo e sulla capacità di produrre fattori pro-angiogenici e cardioprotettivi di tali cellule. Lo scopo è quello di individuare molecole che possiedono un effetto benefico sulle hCPCs e di sviluppare nuovi protocolli di pre-condizionamento per migliorare il loro potenziale terapeutico. Studi in-vitro ed in-vivo suggeriscono come una alterazione del pool delle hCPCs sia associata allo sviluppo e alla progressione di diverse cardiomiopatie. È quindi interesse del nostro laboratorio studiare il coinvolgimento delle hCPCs in alcune patologie croniche, come la fibrillazione atriale.
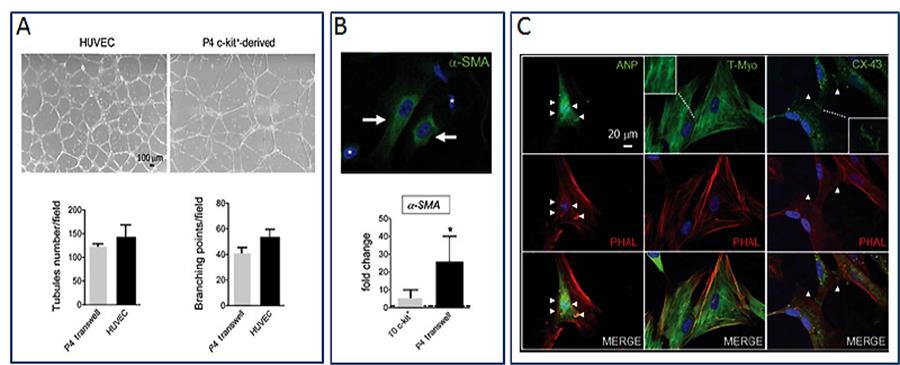
(Sopra) Le hCPCs in opportune condizioni di coltura sono in grado di differenziare (A) formando tubi su una matrice sintetica (tipici del differenziamento endoteliale), (B) esprimendo α-SMA, marcatore tipico delle cellule muscolari lisce e (C) esprimendo ANP, T-Myo e CX-43, marcatori tipici cardiomiocitari. Da: Gambini et al., Car Res, 2011.
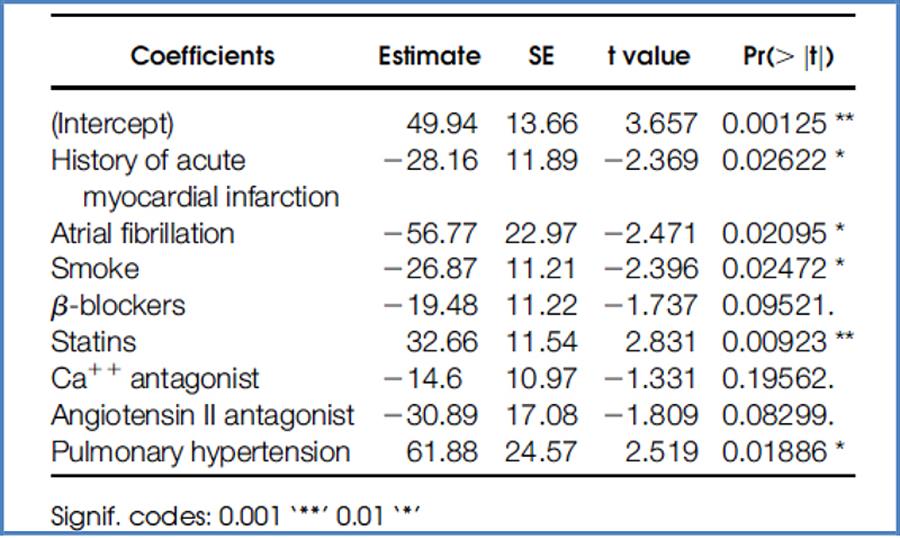
(Qui a lato) Mediante una analisi di regressione lineare con metodo di selezione stepwise è stata individuata l’associazione tra variabili cliniche e demografiche dei pazienti e le caratteristiche biologiche delle hCPCs. Dall’analisi è emerso come la capacità proliferativa delle hCPCs sia significativamente ridotta in presenza di fibrillazione atriale e aumentata con l’assunzione di farmaci quali le statine. Da: Gambini et al., Trals Res, 2012.
Studio dei meccanismi epigenetici e molecolari della disfunzione dei progenitori vascolari nelle patologie metaboliche
Le cellule staminali adulte esistono e funzionano fisiologicamente nei nostri tessuti. La loro elevata capacità proliferativa e propensione a differenziarsi in tipi cellulari specializzati costituiscono “il principio attivo” della terapia rigenerativa. E’ a queste competenze che l’Unità di Biologia Vascolare e Medicina Rigenerativa guarda con attenzione con l’intento di implementarne le capacità a scopi terapeutici. Purtroppo la presenza di patologie metaboliche come obesità, iperomocisteinemia e diabete mellito riduce notevolmente la loro funzionalità.
Questo preclude l’impiego autologo di queste cellule in medicina rigenerativa ed è causa dell’insorgenza di numerose complicanze a livello di tessuti ed organi. Tra queste, le complicanze vascolari, annoverate tra le più serie manifestazioni della patologia diabetica, sono responsabili dell’aumento di rischio d’infarto miocardico, ictus e di amputazioni non traumatiche degli arti inferiori. Le cellule staminali maggiormente coinvolte in questo processo sono i progenitori endoteliali (EPCs ), cellule di derivazione midollare che partecipano alla neovascolarizzazione postnatale e al mantenimento dell’omeostasi vascolare. Il loro numero e funzionalità sono infatti notevolmente ridotte nei soggetti diabetici.
Nonostante il crescente numero di sforzi volti a ripristinare le funzioni delle cellule staminali, i meccanismi molecolari alla base della loro disfunzione sono ancora poco conosciuti. L’obiettivo della nostra Unità è di studiare su base epigenetica i meccanismi molecolari che in concerto contribuiscono all’insorgenza e al mantenimento del fenotipo disfunzionale delle cellule staminali nelle malattie metaboliche.
I risultati potrebbero portare all’identificazione di nuove strategie terapeutiche atte a migliorare o ripristinare la funzionalità delle cellule staminali, anche per il loro impiego autologo nella medicina rigenerativa. Inoltre, poiché la strategia più potente per ridurre la morbilità / mortalità cardiovascolare associata alle malattie metaboliche è rappresentata da una diagnosi precoce, l'identificazione delle modificazioni epigenetiche ad esse associate potrebbe fornire nuovi marker per l’individuazione precoce di soggetti suscettibili ad eventi patologici cardiovascolari.
Studi pre-clinici di prodotti di terapia cellulare cardiaca e traslazione clinica GMP-grade
La medicina rigenerativa basata sull’impiego di cellule staminali/progenitrici di origine cardiaca ha fornito approcci terapeutici alternativi nel trattamento delle patologie cardiovascolari. Tuttavia, studi preclinici hanno dimostrato che le hCPCs presentano una limitata capacità di sopravvivenza, proliferazione e integrazione nel cuore danneggiato. Lo sviluppo di tecniche che migliorino la sopravvivenza delle hCPCs trapiantate è fondamentale per ricostituire in modo adeguato il pool di cellule staminali residenti e per massimizzare il loro potenziale rigenerativo. Di conseguenza, nostro interesse è quello di testare l’efficacia terapeutica delle hCPCs studiate finora nel nostro laboratorio in modelli preclinici di ischemia acuta e cronica del miocardio per identificare le sottopopolazioni con migliore capacità rigenerativa.
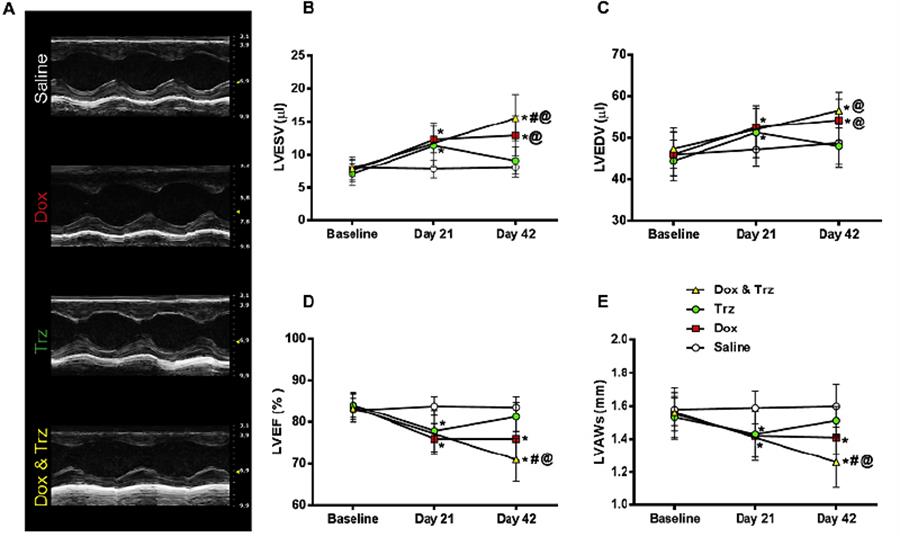
Per questi studi ci avvaliamo della vasta esperienza dell’Unità su modelli murini di patologie cardiache e di ischemia periferica e su tecnologie avanzate di analisi funzionale cardiaca, come l’ecocardiografia 2-D, misurazioni emodinamiche invasive del ventricolo sinistro e destro, e l’analisi perfusionale con laser doppler. L’Unità ha inoltre vasta esperienza in modello cardiaco ex-vivo di perfusione isolata di Langendorff.
Di seguito un esempio di analisi ecocardiografica a carico del ventricolo sinistro a seguito di induzione di disfunzione cardiotossica.